サレド®カプセル 25・50・100
- 製品基本情報
- 製剤写真
- 市販後の安全性情報(副作用)
- 製造販売後調査
製品基本情報
| 製品名 | サレドⓇカプセル25/サレドⓇカプセル50 /サレドⓇカプセル100 |
| 一般名 | サリドマイド |
| 添付文書 | 2025年05月改訂(第5版) |
| インタビューフォーム | 2025年05月改訂(第15版) |
| くすりのしおり | くすりのしおり |
| 患者向医薬品ガイド | 2025年06月更新 |
| 適正使用情報 | ~ENL治療にあたって~(らい性結節性紅斑)(2025年05月改訂第4版) |
包装・製品コード
| サレドⓇカプセル25 | サレドⓇカプセル50 | サレドⓇカプセル100 | |
| 販売包装単位 | (PTP)7カプセル✕4 | (PTP)7カプセル✕4 | (PTP)7カプセル✕4 |
| 薬価基準収載医薬品コード(YJコード) | 4291019M3026 | 4291019M2020 | 4291019M1023 |
| レセプト電算処理システム用コード | 622267801 | 621984001 | 620008558 |
| 基準番号(HOTコード) | 1226782010101 | 1198409010101 | 1189346010101 |
| 統一商品コード | 196402206 | 196401209 | 196400202 |
| GS1 調剤包装単位コード | 04987196191346 | 04987196620716 | 04987196125570 |
| GS1 販売包装単位コード | 14987196402203 | 14987196401206 | 14987196400209 |
製剤写真
サレドⓇカプセル25
| 剤形 | PTP |
 |  |
サレドⓇカプセル50
| 剤形 | PTP |
 |  |
サレドⓇカプセル100
| 剤形 | PTP |
 | 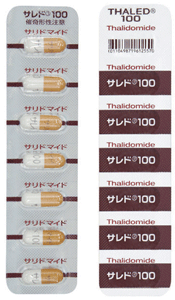 |
市販直後調査
製造販売後調査
サレド®カプセル製造販売後調査の概要
サレドⓇカプセル25・50・100は、以下の承認条件が付与されています。
承認条件
クロウ・深瀬(POEMS)症候群
国内での治験症例が極めて限られていることから、製造販売後、一定数の症例に係るデータが集積されるまでの間は、全症例を対象に使用成績調査を実施することにより、本剤の使用患者の背景情報を把握するとともに、本剤の安全性及び有効性に関するデータを早期に収集し、本剤の適正使用に必要な措置を講じること。
藤本製薬株式会社では、承認条件を踏まえ、以下の調査を実施いたします。
医療関係者の皆様には、製造販売後調査にご協力を賜りますようよろしくお願い申しあげます。
【製造販売後調査に関するお問い合わせ先】
藤本製薬株式会社
ファーマコビジランス部
E-mail:pms@fujimoto-pharm.co.jp
